如果不用复杂的蛋白结构,仅依靠一种简单的金属材料,能否实现类似酶的功能?这个看似“反常识”的问题,正在被材料科学重新回答。

传统人工核酸酶通常依赖精密的分子设计,例如多金属中心或复杂配体结构来实现对DNA的识别与切割。然而,该研究提出了一种完全不同的思路:仅依赖液态镓(Ga)微/纳米液滴,即可实现DNA剪切功能。 如图1所示,这些液态镓液滴在水和氧存在条件下即可表现出核酸酶样活性,并且具有一定的序列偏好性——优先切割 T-T 和 A-A 位点。这一结果突破了传统 “结构决定功能”的人工酶设计范式,展示了元素级材料也可以具备选择性生物功能。
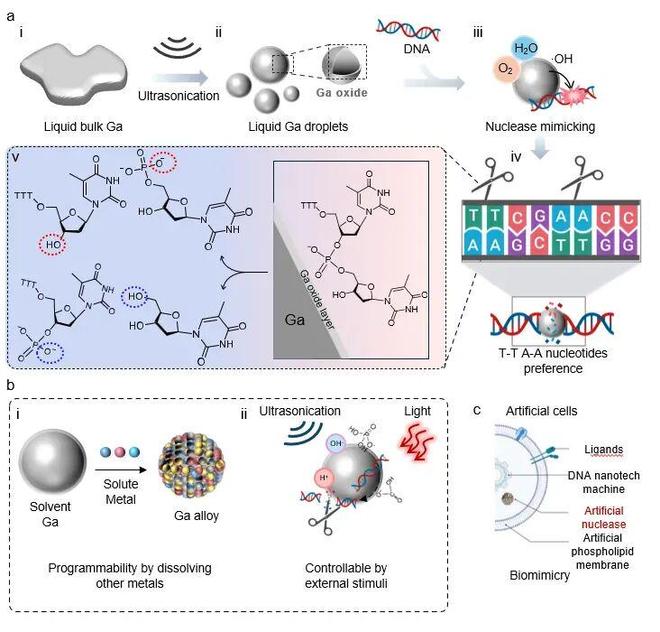
这一体系的核心不在于“材料本身”,而在于其动态界面行为。整体机制可以分为三个关键步骤 :
• DNA界面吸附: 液态镓表面的氧化层(如Ga₂O₃/GaOOH)首先作为 “平台”,通过静电作用与范德华力将DNA分子吸附并富集到界面。
• 界面原位生成ROS: 在水和氧的参与下,液态镓表面发生电子转移反应,生成多种活性氧物种(ROS),其中以羟基自由基(·OH)为主导活性物种。
• ROS介导的水解断裂: 不同于传统Fenton体系中对碱基的随机氧化,该体系主要通过·OH参与的磷酸二酯键水解实现DNA断裂,更接近天然核酸酶的作用方式。
研究的一个关键发现是:固态镓几乎不具备该活性,而液态状态是功能产生的前提。其本质原因在于液态镓具备:1) 动态重构的界面(持续暴露新活性位点); 2) 高密度自由电子(支持持续电子转移); 3) 可破裂/再生的氧化层结构。这些特性共同构成一个“自更新”的反应界面,使得ROS能够持续生成,从而维持核酸酶样活性。
除了基础活性之外,该体系还表现出高度的可调控性:1) 通过调节液滴尺寸改变反应效率 ; 2) 通过合金化调控界面化学性质 ;3) 通过外部刺激(如超声、激光、pH变化)实现活性增强或调控。 这意味着该体系不仅是一个“功能材料”,更是一个可设计、可编程的人工酶平台。
这一工作的重要性,不仅在于“发现了一种新型核酸酶”,更在于提出了一种新的科学范式:
• 极简人工酶设计(Minimalist enzyme mimic): 传统人工酶通常依赖复杂的分子结构与精细的化学修饰,而该研究表明,仅通过简单的元素级材料与界面调控,即可实现类似酶的功能,为低复杂度、高可拓展性的人工酶设计提供了新路径。这种“去复杂化”的策略有望降低人工酶体系的设计门槛,并提高其在实际应用中的可实现性。
• 界面驱动的生物化学反应: 该体系将“功能来源”从分子结构转移到材料界面,强调电子转移、界面吸附与局部反应环境在生物化学过程中的核心作用,为理解和设计新型催化体系提供了不同于传统分子催化的视角。这一机制也为开发新型反应平台(如界面催化、生物界面工程)提供了理论基础。
• 非生命系统的类生命行为: 简单的无机材料体系能够表现出选择性、可调控甚至类似“功能分工”的行为,体现出一定程度的类生命特征,为构建人工生命系统与合成生物体系提供了新的基础单元。
博士生刘丽(悉尼大学,负责主要实验)、博士生芦溪(南安普顿大学,负责机理探索和分析)和郑杰伟博士(皇家墨尔本理工大学,负责理论计算)为本文共同第一作者(排名不分先后)。
张成晨博士课题组一直致力于研究基于镓的液态金属与生物分子之间的相互作用及其机理,并探索其在生物医学领域的应用. 目前课题组正在招收一名全奖博士(2026年秋入学)和一名博后(1年,可延长至2年,需具备理论计算背景)。 欢迎有兴趣的同学联系咨询详情。